Роль пищеварительной системы в предупреждении старения
Поиск факторов, влияющих на старение, и стратегий борьбы с ним является одной из наиболее актуальных проблем интегративной и превентивной медицины. И здесь особая роль принадлежит пищеварительной системе, поскольку нарушения в ее работе неминуемо влияют на работу всех других органов, в том числе самого большого из них — кожи.
Лариса Гладских,
д. фарм. н., академик Российской академии медико-технических наук, г. Москва
Известно, что организм человека существует до тех пор, пока в нем сохраняется баланс сил, созидающих и разрушающих. Действительно, специфическими чертами процессов жизнедеятельности является непрерывный распад и синтез веществ, функциональное напряжение, покой и т.д. Эти взаимно противоположные по своему характеру процессы участвуют в регенерации (обновлении) функционирующих структур организма, который располагает двумя основными стратегиями замены собственных поврежденных тканей и самообновления [1].
Непрерывное обновление на самом деле представляет собой основу функционирования организма. А изменение этого баланса обусловливает морфофункциональные изменения организма человека, что способствует развитию многих патологических состояний и преждевременному старению.
Следует отметить, что на фоне существующего множества теорий старения особого внимания заслуживает теория износа организма человека вследствие двух основных причин: нарушения функций пищеварительной системы и присутствия в организме очагов хронической инфекции. Подтвержденная научными данными и результатами практической работы, эта теория предлагает эффективный путь профилактики преждевременного старения и снижения риска развития хронической патологии [2].
Безусловно, значение пищеварительной системы для здоровья человека невозможно переоценить, поскольку от функционирования ее органов зависит эффективность поддержания трофики и жизнедеятельности всех органов и систем в целом, а с другой стороны — степень нейтрализации негативно воздействующих факторов внешней среды.
Иными словами, пищеварительная система является особой высокоспециализированной системой, осуществляющей в результате сложных биохимических и физических процессов доставку энергии, строительного материала к клеткам организма человека, обеспечивающей также их адаптацию и защиту от различных вредных воздействий внешней среды.
При несостоятельности пищеварительной системы и невозможности пополненияn энергетических и пластических ресурсов организма за счет метаболизма различных пищевых веществ и собственного синтеза развиваются различные метаболические нарушения с последующим формированием многих заболеваний неинфекционного происхождения [3].
Мы живем в эпоху эволюционного несоответствия, поскольку жизненный уклад разных народов подвергается непрерывной ломке, изменяются и условия жизни современного человека (особенно по сравнению с теми, к которым готовила его эволюция), и организм человека не успевает приспосабливаться к новым условиям. В XX веке такие изменения имели особенно бурный характер, и естественно, это не произошло без ущерба для здоровья людей. Причем бóльшую долю в статистике заболеваемости занимает хроническая патология, обусловленная изменением образа жизни, включая нерациональное питание современного человека.
К началу ХХI столетия сформировались нездоровые структура и режим питания, послужившие пусковым механизмом для развития дезадаптационного синдрома, который с учетом увеличения продолжительности жизни населения в индустриально развитых странах Европы и Запада способствовал реализации повышенного риска генетически обусловленных заболеваний, формированию сердечно-сосудистой патологии, сахарного диабета и рака. Так, по данным ВОЗ, неадекватное питание обеспечивает риск развития хронической патологии в 50% случаев всех зафиксированных смертей. Степень современных знаний о человеке позволяет рассматривать его с позиций симбиоза с многочисленными и разнообразными микроорганизмами, совокупность которых обозначается как микробиом. Концепция того, что кишечная микробиота модулирует многочисленные физиологические процессы, включая развитие и функционирование иммунитета, питание и метаболизм, не в полной мере принимается в научном сообществе.
Микробы встроены в нашу биологическую систему и глубоко интегрированы в повседневную жизнь, поэтому произошел сдвиг в сторону понимания механизмов, посредством которых изменение микробиоты может приводить к появлению болезни [4]. Уточнение этих механизмов может дать информацию при разработке новых методов лечения и оптимизировать клиническую практику.
Известно, что кишечная микробиота обладает множеством функций, которые влияют на ее способность расти и колонизировать разные биотопы, в то же время вызывая биологические эффекты для организма человека, которые могут быть полезными или негативными. Поскольку желудочно-кишечный тракт человека не способен переваривать некоторые компоненты пищевых волокон из-за отсутствия необходимых ферментов для расщепления и использования энергии углеводов, некоторые виды кишечной микробиоты обеспечивают их ферментацию в короткоцепочечные жирные кислоты. Короткоцепочечные жирные кислоты в организме человека могут оказывать противовоспалительное и иммуномодулирующее действие. Короткоцепочечные жирные кислоты играют решающую роль во взаимодействии между диетой, микробиотой кишечника и последующей активацией или ингибированием воспалительных каскадов. Кроме того, они способствуют гомеостатическому контролю энергии, регуляции аппетита за счет своего воздействия на метаболические пути.
Особое внимание уделяется микробному метаболиту, который ингибирует метаболические пути, ведущие к выработке противовоспалительных цитокинов, — бутирату. Кроме того, бутират минимизирует транслокацию липополисахаридов в кишечнике, тем самым снижая эффекты, связанные с их негативным действием.
Другая группа бактериальных метаболитов — производные аминов, включая триметиламин N-оксид (ТМАО), который является наиболее известным и изученным из всех моноаминов. Диетический холин, карнитин и бетаин, соединения, присутствующие в красном мясе, рыбе и других источниках животного происхождения, метаболизируются микробами кишечника в триметиламин (ТМА), который затем превращается в ТМАО под действием ферментов печени. Присутствие ТМАО в крови в высоких концентрациях способствует развитию сердечно-сосудистой патологии [4].
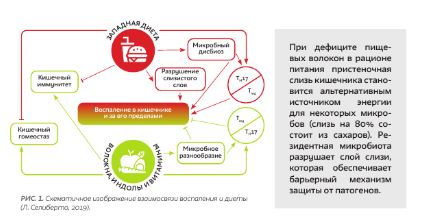
Следует отметить, что кроме метаболизма питательных веществ кишечные микроорганизмы обеспечивают естественную защиту от патогенных видов бактерий за счет конкуренции и поддержания целостности слизистой оболочки. Именно через их контакт с иммунной системой они могут вызывать или предотвращать воспаление. У людей, придерживающихся диеты западного типа, возникают дисбиоз, повреждение слизистого барьера кишечника, изменение баланса провоспалительных противовоспалительных Т-клеток. Эти нарушения приводят к воспалению в кишечнике и за его пределами (рис. 1). Несбалансированное питание приводит к уменьшению количества полезных микробов и размножению микроорганизмов, которые ослабляют ключевые факторы защиты и барьерную функцию кишечника, тем
самым способствуя развитию хронического воспаления в кишечнике [5].
Восстановление здоровья начинается нормализации кишечного звена — ворот нашего организма, непосредственно контактирующих с защитной системой, которая
Продуцирует провоспалительные сигналы, как сигнал бедствия распространяющиеся во все органы.
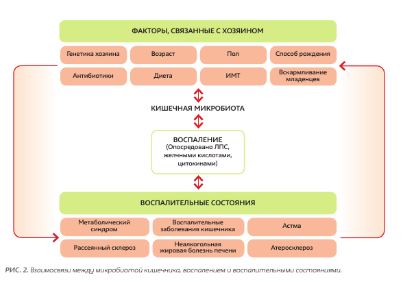
Воспаление лежит в основе многих хронических мультисистемных состояний, включая ожирение, атеросклероз, сахарный диабет 2-го типа и воспалительное заболевание кишечника [6]. Воспаление может быть вызвано структурными компонентами бактерий, что может привести к каскаду воспалительных путей с участием интерлейкинов и других цитокинов. Микробиота кишечника имеет двунаправленную связь с воспалением и в зависимости от своего состава может ингибировать или стимулировать воспалительные пути (рис. 2).
Таким образом, микробные метаболиты являются регуляторами состояния здоровья и старения нашего организма. Нормализуя кишечную микробиоту, мы можем замедлить наши биологические часы.
Очевидно, что здоровье человека можно сравнивать с цепью, состоящей из многочисленных звеньев, одним из которых является кишечник. К сожалению, значение этого органа часто сужают до его пищеварительных функций, считают второстепенным, в то время как его роль можно без преувеличения сопоставить с функциями «второго мозга». Кишечная экосистема поддерживает важные взаимосвязи с определенными органами, такими как мозг, печень и кожа. Следовательно, любые функциональные нарушения в кишечнике могут отражаться на связях с этими органами.
Современные знания включают изучение взаимодействия в рамках «Ось кишечник — кожа» — это биохимическая сигнализация, которая происходит между желудочно-кишечным трактом и кожей. «Ось кишечник — кожа» здесь относится к двунаправленным взаимодействиям между тканями кожи и микробиотой кишечника с конечной целью модулирования иммунного ответа [7].
Кожные заболевания являются результатом сложного взаимодействия между генетической предрасположенностью, образом жизни и иммунной системой. В частности, последняя находится в постоянном взаимодействии с нервной и эндокринной системами. Эти взаимодействия позволяют микробиоте играть ключевую роль, особенно в таких органах, как кожа и кишечник, которые насыщены иммунорегуляторами и микробиотой.
Пищеварительная система и кожа
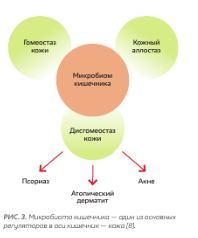
Для врачей-косметологов важно понимать связь между кожей, которая является основным объектом их профессионального интереса, и органами пищеварения, поскольку нарушение в работе последних является триггером развития таких сложных воспалительных заболеваний акне, розацеа, псориаз, атопический дерматит и тому подобных (рис. 3).
Исследования, проводимые на эту актуальную тему, также подтвердили наличие связи между динамикой микробов, кожным барьером и процессом старения [8]. Микробиота влияет на дифференциацию и кератинизацию кожи, а также на модуляцию кожного иммунного ответа при различных заболеваниях [8].
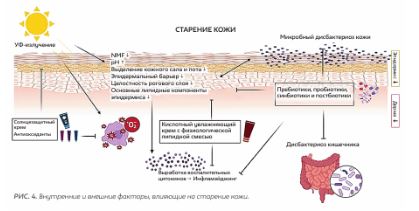
Связь микробиоты кишечника и эпидермального барьера кожи позволяет моделировать систему оси «кишечник — кожа» с помощью пероральных препаратов (корригирующих дисбиоз, нейтрализующих негативное действие окислительного стресса) и локальных средств, предупреждающих развитие возрастных изменений кожи (рис. 4). Кишечная микрофлора определяет значительный вклад в общее состояние организма человека, как модулируя метаболизм и формируя иммунитет, так и формируя тканевую функциональность кожи, обладающей собственным микробиомом.
Микробиологические дисбалансы в таком случае нарушают гомеостатическое равновесие и могут ускорять возрастные изменения кожи, изменяя резистентность ткани к внешним воздействиям и ускоряя процессы старения (рис. 4).
Поэтому по-настоящему эффективным будет лишь комплексный подход к лечению воспалительных заболеваний кожи. В условиях изменившегося в процессе эволюции пищевого поведения зачастую недостаточно лишь локальными средствами работать только с кожей. Это приводит специалиста к необходимости рассматривать организм как единое целое для достижения действительно стойкого результата. Персонализированный подход включает в себя аналитику каждого конкретного случая и сочетание профилактических мер, актуальных для определенного пациента с его группами риска, отслеживание и своевременную коррекцию изменений системы желудочно-кишечного тракта у смежных специалистов и учет генетических предрасположенностей. Разумеется, важнейшим аспектом работы будет и санитарно-просветительская работа с целью минимизировать пагубное воздействие факторов внешней среды.
Выводы
С помощью современной науки мы можем отсрочить развитие многих хронических заболеваний, которые ассоциированы возрастными изменениями. Сегодня наука рассматривает кожу как один из органов мощной биологической системы, локально работая с которым, невозможно получить долгосрочные хорошие результаты. Во всем мире декларируется системный подход к здоровью кожи с учетом необходимости противодействовать внутренним механизмам, способным вызывать преждевременное старение и увеличивать риск побочных эффектов. Таков современный взгляд на роль пищеварительной системы в предупреждении старения человека и, как следствие, в достижении красоты и здоровья кожи.
ЛИТЕРАТУРА
- Общая патология человека. Руководство. Под ред. Струкова А.А., Серова В.В., Саркисова Д.С. — М.: Медицина, 1982
- Ролик И.С. Основы клинической фармакологии органопрепаратов. Руководство. — М.: РегБиоМед, 2004
- Максимов В.И. Пища и дегенеративные болезни. / Максимов В.И. — М.: Миклош, 2010
- Al Bander Z., Nitert M.D., Mousa A., Naderpoor N. The gut microbiota and inflammation: an overview. Int J Environ Res Public Health. 2020 Oct 19; 17(20): 7618
- Siracusa F., Schaltenberg N., Villablanca E.J., et al. Dietary Habits and Intestinal Immunity: From Food Intake to CD4+ T H Cells. Front Immunol. 2019 Jan 15; 9: 3177
- De Pessemier B., Grine L., Debaere M., et al. Gut–Skin Axis: Current Knowledge of the Interrelationship between Microbial Dysbiosis and Skin Conditions. Microorganisms 2021, 9 (2), 353
- Woo Y.R., Kim H.S. Interaction between the microbiota and the skin barrier in aging skin: a comprehensive review. Front Physiol. 2024 Jan 19; 15: 1322205
- Salem I., Ramser A., Isham N., Ghannoum M.A. The gut microbiome as a major regulator of the gut-skin axis. Front Microbiol. 2018 Jul 10; 9: 1459



 Сайт может содержать материалы, предназначенные для лиц старше 18 лет
Сайт может содержать материалы, предназначенные для лиц старше 18 лет
