Применение нейропротеина типа А в дерматологии с терапевтическими целями: систематический обзор
Emanuela Martina, Federico Diotallevi, Giulia Radi, Anna Campanati, Annamaria Offidani клиника дерматологии, кафедра клинических и молекулярных наук, Политехнический университет Анконы, Италия
ИСТОЧНИК Martina E, Diotallevi F, Radi G, Campanati A, Offidani A. Therapeutic Use of Botulinum Neurotoxins in Dermatology:Systematic Review // Toxins (Basel). 2021;13(2):120. doi:10.3390/toxins13020120Статья печатается с сокращениями
В последнее время ботулинический нейропротеин типа А, помимо официальных показаний, используют для лечения многих заболеваний кожи. Итальянские учёные задались целью собрать и проанализировать сведения о самых распространённых официальных и неофициальных показаниях к использованию нейропротеина типа А в дерматологии. Авторами составлен систематический обзор опубликованных данных в соответствии с рекомендациями PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses, «Предпочтительные моменты для представления результатов систематических обзоров и метаанализов»).
ИДИОПАТИЧЕСКИЙ ГИПЕРГИДРОЗ
Идиопатический гипергидроз — хроническое вегетативное нарушение, характеризуемое излишней выработкой пота. Это сильно ухудшает качество жизни, приводя к неловкости в социальных ситуациях, мешая в профессиональной деятельности, на физическом и психологическом уровнях.
Очаговый и множественный идиопатический гипергидроз встречается и у детей. В настоящее время причины его возникновения изучены плохо. Пациенты часто упоминают его в семейном анамнезе, что наводит на мысли о генетической предрасположенности. Так выявлено наличие наследственного варианта, передающегося по аутосомно-доминантному признаку, выраженному в виде аномалии в хромосоме 14q.
Идиопатический гипергидроз обычно начинается в детстве. Страдают им 0,6 – 1 % населения. Диагностическим показателем для него являются чрезмерная потливость, сохраняющаяся не менее полугода без очевидных причин, плюс не менее двух из следующих явлений: возникновение при повседневной деятельности; симметричность; пер- вые проявления в возрасте до 25 лет; отсутствие очагового потоотделения во время сна; положительный семейный анамнез.
Диагноз «идиопатический гипергидроз» может рассматриваться только после исключения вторичных причин излишней потливости, таких как приём определённых лекарств, поступление в организм токсических веществ, а также наличие системных заболеваний (эндокринного, неврологического или метаболического характера), злокачественных новообразований. В 90 % случаев идиопатический гипергидроз проявляется в области подмышек, ладоней, подошв, а также волосистой части головы и лица.
В настоящее время для его лечения существует несколько методов. Чаще всего при идиопатическом гипергидрозе от слабой до средней степени выраженности применяют гексагидрат хлорида алюминия. Однако использование местных средств обладает недостатками — такими как возможное возникновение раздражения или аллергического контактного дерматита либо кратковременный результат.
Впервые уменьшение потоотделения под действием инъекций нейропротеина типа А наблюдалось у волонтёров без яркой симптоматики заболевания. Инактивируя SNARE-белки, ботулинический нейропротеин (БНП) препятствует высвобождению ацетилхолина и ряда других нейротрансмиттеров из пресинаптических пузырьков. Деятельность эккриновых потовых желёз регулируется ацетилхолином, соответственно, инъекции БНП уменьшают секрецию пота. Интрадермальное введение для лечения гипергидроза обычно выполняется в виде сетки иглой малого калибра (30G) на глубину в несколько миллиметров, по 2 – 2,5 ЕД препарата на вкол. В качестве недостатка пациенты чаще всего отмечают боль от инъекций в момент вкола, особенно в области ладоней и стоп. Есть методы, позволяющие обойти эту проблему: может использоваться топическая анестезия, в том числе криоанестезия*, виброанестезия, блочные микроиглы, седация, проводниковая анестезия.
Skiveren et al. изучили, как размер иглы влияет на боль от инъекций БНП, сравнив иглы калибра 27G и 30G. Согласно результатам исследования, сама по себе травма кожи иглой может быть не главным источником боли. Авторы поддерживают гипотезу о том, что боль вызывают другие факторы, такие как гидростатическое давление на окружающие ткани и активация болевых рецепторов веществами в составе вводимого препарата.
Инъекции ботулинического нейропротеина типа А в области подмышек весьма эффективны, безопасны и хорошо переносятся пациентами. Ряд исследований подтверждает, что инъекция 50 ЕД БНП в каждую подмышечную впадину позволяет эффективно бороться с идиопатическим гипергидрозом. Marcella et al. отметили, что доза в 35 ЕД в каждую подмышечную впадину может быть эффективна у женщин с умеренно выраженным гипергидрозом, что означает возможность индивидуального подбора схемы лечения, а не наличие «универсальной» дозировки. Исходя из этих результатов, установленный уровень доказательности (уровень А) позволяет использовать инъекции БНП в качестве монотерапии при лечении идиопатического гипергидроза подмышек.
Что касается продолжительности облегчения симптомов идиопатического гипергидроза, эффект ботулинического нейропротеина при использовании в данной области сохраняется в течение 4 – 9 месяцев (D'Epiro et al. сообщают о среднем периоде в 7,2 месяца). Чаще всего при повторных инъекциях длительность эффекта нейропротеина типа А возрастает. Так, Lecouflet et al. опубликовали исследование на 83 испытуемых с идиопатическим гипергидрозом подмышек и сообщили о статистически значимом увеличении длительности эффекта при последующих инъекциях. Авторы отметили аналогичные результаты у 23 пациентов с идиопатическим гипергидрозом ладоней. По их предположениям, такое увеличение длительности действия и эффективности повторных инъекций связано с постепенной регенерацией терминалей аксонов двигательных нейронов. Berthin и Maillard недавно подтвердили эти предположения на основании ретроспективного исследования на 117 пациентах, охватывающего период в 15 лет.
В качестве альтернативы ботулинотерапии при лечении идиопатического гипергидроза подмышек предложена тумесцентная липосакция, основанная на сепарации тканей с помощью тупоконечной канюли на уровне дермально-гиподермального соединения, где располагается большая часть потовых желёз. Ibrahim et al. провели прямое сравнительное исследование на 20 испытуемых. Оказалось, что инъекции нейропротеина типа А имеют значительное статистическое преимущество перед методиками с использованием тупоконечной канюли. Период наблюдений составил шесть месяцев. Пациенты также указывали на предпочтительность терапии БНП.
Идиопатический гипергидроз ладоней — тяжёлое заболевание неизвестной этиологии, хотя есть данные о гиперактивности симпатических нервных волокон, проходящих через грудные симпатические ганглии Т2 и Т3. Для лечения такого локального гипергидроза предложены местные средства, ионофорез, оксибутинин перорально или хирургическое вмешательство. Антихолинергик оксибутинин используется для лечения гипергидроза, особенно множественного или генерализованного. Хлорид оксибутинина показан людям, страдающим гиперактивностью мочевого пузыря нервного или рефлекторного характера. Однако всё чаще в литературе говорится и о терапевтическом применении оксибутинина при первичном гипергидрозе, дозой в 5 – 15 мг ежедневно. Среди относительно слабо выраженных побочных эффектов — сухость во рту, головная боль, запор и задержка мочи, особенно когда его ежедневная доза достигает 15 мг.
Имеющиеся исследования указывают на то, что безопасность и эффективность оксибутинина при гипергидрозах позволяют комбинировать его с терапией с помощью БНП. В частности, авторы данного исследования изучили эффективность последовательного применения хлорида оксибутинина перорально после инъекций БНП в сравнении с монотерапией хлоридом оксибутинина у лиц, страдающих первичным гипергидрозом ладоней. Был также рассмотрен вопрос, позволяет ли такой последовательный подход уменьшать проявления гипергидроза за счёт меньших доз перорального оксибутинина. Согласно результатам, комбинированная терапия избавляет пациентов от симптомов заболевания на целых 52 месяца (при удовлетворительной безопасности и меньшем количестве побочных эффектов), тогда как одни лишь инъекции БНП дают результат длительностью 2 – 8 месяцев. В случаях тяжёлого гипергидроза, если другие методы не принесли результатов, предлагается хирургическое лечение (симпатикотомия и торакальная симпатэктомия), однако неприятным побочным явлением в этом случае может стать компенсаторный гипергидроз других областей.
В отношении применения ботулинического нейропротеина типа В для лечения идиопатического гипергидроза ладоней существуют разногласия относительно конверсии дозировки и степени его диффузии по сравнению с нейропротеином типа А. Basciani et al. предлагают использовать общую дозу в 5000 ЕД (rimabotulinumtoxin b) на одну ладонь, восстановленных в 10 мл 0,9 %-ного раствора хлорида натрия.
В клинической практике для лечения вегетативных нарушений чаще всего используется коэффициент конверсии в 1 : 50...100. Лечение гипергидроза с помощью БНП-В изучено пока в небольшом количестве исследований по сравнению с лечением БНП-А. Такая существенная разница, вероятно, связана с более высоким риском иммуногенности ввиду большего содержания чужеродного белка в общей дозировке вводимого препарата. На иммуногенность ботулинического нейропротеина влияют многие факторы, в том числе связанные с самим продуктом (производство, источник действующего вещества, степень очистки, количество белка, общая антигенная нагрузка, эксципиенты), с процессом лечения (доза, интервалы между сеансами лечения), предшествующими инъекциями и прививками либо с принимающим организмом (генетическая предрасположенность).
Поскольку первичный гипергидроз носит хронический характер, очень важно донести до пациента важность поддержания эффективности на дальнейших сеансах. Высокие дозы нейропротеина типа А, вводимые интрадермально за один сеанс, также повышают риск проявления системных неврологических побочных эффектов. Kouris et al. описывают случай у молодой женщины, получившей за один сеанс общую дозу в 400 ЕД ботулинического нейропротеина типа А для лечения гипергидроза ладоней и почувствовавшей через три дня головокружение, головную боль, тошноту, слабость и боль в мышцах, невозможность опереться на что‑либо, трудности с открыванием глаз и концентрацией взгляда, а также сонливость. Симптомы постепенно ослаблялись и спустя шесть недель полностью исчезли. Генерализованные симптомы можно объяснить локальным захватом аксонами и ретроградным транспортом через спинальные мотонейроны либо системным распространением через кровоток. Другие факторы, которые могут способствовать системным побочным эффектам: высокая частота сеансов, неверное техническое исполнение, идиосинкразия, генетическая предрасположенность, недостаточность веса, гендерные и анатомические различия в строении ладоней. Обычная схема инъекций ботулинического нейропротеина типа А предполагает использование 100 ЕД, восстановленных в 5 мл 0,9 %-ного раствора хлорида натрия. Инъекции проводятся интрадермально в каждую ладонь, распределение равномерное, примерно в 25 точек. Длительность эффекта в различных исследованиях отмечается разная, от двух до 22 месяцев, в зависимости, в основном, от дозировки. В качестве побочного эффекта часто встречается временная слабость мышц большого пальца (пациенту сложно брать предметы в руку). Есть интересное исследование на эту тему, проведённое на большой популяции (474 пациента). Результаты показали, что слабость мышц была вторым по распространённости побочным эффектом в течение первой недели после инъекции, причём у женщин она встречалась вдвое чаще, чем у мужчин. Объяснение, предлагаемое авторами, связывает это явление с анатомическими различиями, а также особенностями работы или хобби у людей разного пола. Эти данные особенно интересны в клинической практике: они подразумевают необходимость корректировки дозы и схемы инъекций на основании пола пациентов.
Лечение гипергидроза стоп даётся труднее, чем на других участках: около 50 % пациентов остаются недовольны. Здесь уколы могут быть болезненнее, а потоотделение заметно уменьшается только через две недели и на более короткий срок по сравнению с другими зонами.
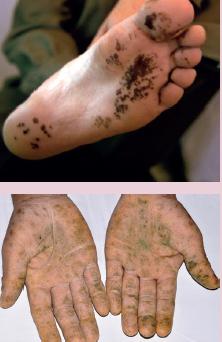
РИС. 1. Клиническая картина хромогидроза.
ХРОМОГИДРОЗ
Хромогидроз — необычное заболевание, проявляющееся выделением окрашенного пота (рис. 1). Он может быть жёлтого, зелёного, голубого или чёрного цвета. Чаще всего явление наблюдается в области лица или подмышек. Это очень неприятное состояние, вызывающее у пациентов неловкость.Об этиопатогенезе заболевания известно мало, до сих пор ведутся споры о том, вызвано ли оно особенностями работы апокриновых или мерокриновых потовых желёз.После первого успешного случая лечения ботулиническим нейропротеином типа А Wu et al. предположили, что болезнь имеет апокринное происхождение, хотя исторически принято считать, что апокринные железы не реагируют на холинергическую стимуляцию ацетилхолином. При этом ввиду выраженной реакции на терапию с помощью БНП Matarasso полагает, что хромогидроз является расстройством мерокринного характера. Если подмышечный хромогидроз можно полностью контролировать за счёт инъекций ботулинического нейропротеина типа А, то в области щёк отмечается резистентность к терапии. Возможно, расхождение результатов основано на разнице в степени восстановления препарата. Протокол лечения в области щёк требует дополнительной стандартизации.
БРОМГИДРОЗ
Бромгидрозом называют заболевание, при котором из‑за взаимодействия между секретом апокринных желёз и бактериями появляется неприятный запах. В исследовании He et al. приняли участие 67 пациентов с бромгидрозом подмышек. В каждую подмышечную впадину вводили по 50 ЕД ботулинического нейропротеина типа А Далее каждый месяц проводился контрольный приём. Исследователи зафиксировали, что у 73,1 % (49/67) пациентов неприятный запах тела исчез за счёт ингибирования потоотделения.
Wu et al. недавно опубликовали результаты перспективного рандомизированного клинического исследования, включающего гистологический анализ потовых желёзу лиц с бромгидрозом подмышек, получавших лечение БНП. Средняя степень выраженности неприятного запаха и среднее количество пота в подмышках у лиц, получавших инъекции нейропротеина типа А, оказались существенно ниже спустя три месяца после процедуры, чем в контрольной группе. Гистологический анализ показал атрофические изменения и гипоплазию апокринных потовых желёз у пациентов, получивших инъекцию. He et al. провели исследование на 53 пациентах со вторичным бромгидрозом подмышек после различных хирургических мероприятий; все они получили инъекции 50 ЕД ботулинического нейропротеина типа А, восстановленного в 2,0 мл NaCl 0,9 %. Средний период ремиссии составил шесть месяцев.
Особенно болезненно реагируют на проявления бромгидроза подростки. В исследовании Wang et al. приняли участие 62 пациента-подростка с первичным подмышечным бромгидрозом, получившие инъекции 50 ЕД ботулинического нейропротеина типа А в каждую подмышечную впадину. Лечение дало удовлетворительный результат (51 из 62 пациентов оценили лечение как хорошее или очень хорошее), но у 38,7 % эффект сохранялся менее четырёх недель.
Ещё одна неприятная проблема как мужчин, так и женщин, — дурной запах в области паха, что также очень плохо сказывается на качестве жизни. Основная его причина — бактериальное обсеменение кожи гениталий или слизистой оболочки влагалища, хотя иногда причина кроется в контакте выделяемого пота и некоторых видов бактерий. Lee et al. описали такой случай: пациентка уже много лет страдала от неприятного запаха из области паха, безуспешно пытаясь решить проблему с помощью антибактериального мыла, парфюмов и антимикробных средств. Генитальные инфекции были исключены. Пациентка получила инъекции ботулинического нейропротеина типа А в 40 точек (по 2,5 ЕД / 0,1 мл на каждую точку) волосистой части зоны паха. На девять месяцев выраженность запаха значительно ослабла.
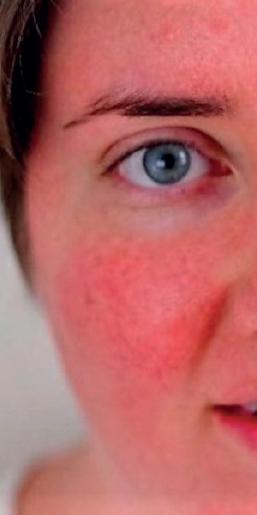
РИС. 2. Клиническая картина гиперемии лица
ЭРИТЕМА И ПРИЛИВЫ
Возможный терапевтический эффект нейропротеина типа А при эритеме и гиперемии лица (рис. 2) обсуждается в нескольких недавних исследованиях, в том числе ряде интересных описаний клинических случаев. Odo et al. провели исследование с целью оценки уменьшения дискомфорта от менопаузных приливов путём интрадермальных инъекций abobotulinumtoxin А Шестидесяти пациенткам, страдающим от менопаузальных приливов, ввели нейропротеин в область волосистой части головы, лица, шеи и декольте в общей дозировке (500 ЕДиниц БНП-А, восстановленных в 3,2 мл физиологического раствора (6,2 ЕД на точку)). Контрольной группе были сделаны инъекции физраствора в том же объёме. Области повышенного потоотделения выявлялись с помощью пробы Минора. Пациенткам было предложено записывать всю информацию, связанную с приливами: их интенсивность, количество эпизодов и подверженные им области. В исследуемой группе спустя 60 дней после процедуры на участках, получивших инъекции БНП, йодокрахмальный тест (проба Минора) был отрицательный, что говорит об отсутствии приливов. Через шесть месяцев после процедуры пациентки стали сообщать о возобновлении излишнего потоотделения, но в меньшей степени, чем изначально. В контрольной группе средняя интенсивность потоотделения и количество приливов не изменились. Несмотря на предположительно удовлетворительные результаты, авторы отметили ряд ограничений исследования: трудность диагностики и обработки всей области, подверженной приливам, а также подтверждения эффективности терапии.
Geddoa et al. провели неконтролируемое исследование 22 пациенток с жалобами на приливы. С помощью ботулинического нейропротеина типа А были обработаны области шеи и декольте. Их разделили на квадраты по 1 см2, в каждый введено по 2 ЕД onabotulinumtoxin A, суммарная дозировка составила 100 ЕД. В начале исследования и на контрольных этапах пациенткам предлагалось заполнить опросник DLQI (Dermatology Life Quality Index, дерматологический индекс качества жизни). Через четыре недели после процедуры качество жизни пациенток существенно повысилось. 20 из 22 пациенток (90 %) сообщили о немедленном улучшении с почти полным исчезновением приливов. Ещё двум женщинам для того же результата потребовалась дополнительная процедура. Нейропротеин типа А является эффективным средством не только при первичных или постменопаузны приливах, но и при плохо поддающихся лечению симптомах у больных розацеа, как показано в описании двух клинических случаев у Park et al. и в обзоре, выполненном Abokwidir et al. В последнее время опубликован ряд исследований, демонстрирующих эффективность сочетания лазерных методов с инъекциями нейропротеина для коррекции эритемы и гиперемии у пациентов с розацеа. Так, Al-Niaimi et al. описали успешный опыт сочетания импульсного лазера на красителях и инъекций нейропротеина типа А интрадермально при эритеме и гиперемии у 20 больных розацеа. Отмечены эффективность метода и высокая степень удовлетворённости пациентов, а также низкая частота побочных эффектов.
Friedman et al. провели ретроспективный обзор случаев 16 пациентов в возрасте от 23 до 45 лет с типами кожи от II до IV по Фицпатрику, страдающих эритематозно-телангиэктатическим розацеа. Они прошли процедуру с использованием термомеханической системы для фракционного омоложения кожи с последующим местным применением 100 ЕД abobotulinumtoxin А В начале исследования, а затем спустя 1, 3 и 6 месяцев после процедуры были выполнены тесты по шкале CEA (Clinicians Erythema Assessment, шкала клинической выраженности эритемы), PSA (Patients selfassessment, шкала самооценки пациента), а также заполнялся опросник DLQI. Результаты оказались значительно лучше спустя шесть месяцев по сравнению с исходными значениями (во всех случаях p < 0,001). Пациенты сообщили о высокой степени удовлетворённости и отсутствии побочных эффектов.
Совокупные исследования о применении ботулинического нейропротеина типа А при этих заболеваниях пока под вопросом; опубликованные исследования дают противоречивые результаты с точки зрения эффективности. Кроме того, трудно объективно оценить непостоянные и субъективные признаки вроде частоты приливов и интенсивности эритемы. Важно и то, что существующие на сегодняшний день исследования отличаются весьма кратким периодом наблюдения и дают минимум данных по долговременной эффективности и безопасности.
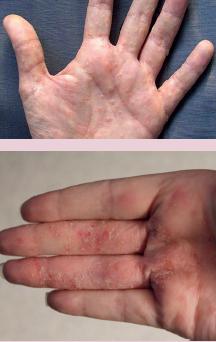
РИС. 3. Клиническая картина дисгидротической экземы.
ДИСГИДРОТИЧЕСКАЯ ЭКЗЕМА
Дисгидротическая экзема — весьма распространённое заболевание, возникающее на ладонях и (или) подошвах. Характеризуется появлением везикуло-буллёзных элементов и трещин, носит хронический и рецидивирующий характер (рис. 3). Этиопатогенез заболевания точно не известен, в настоящее время оно считаетс возможным проявлением атопии или контактного дерматита. Чаще всего симптомы появляются из‑за частого контакта с влагой и моющими средствами, при избыточной потливости, использовании «недышащих» средств защиты. Пациенты жалуются на боль, зуд, ощущение жжения и сильный дискомфорт от перчаток или обуви. Возможно присоединение бактериальных или грибковых инфекций, осложняющих клиническое состояние. В настоящее время существует несколько методов лечения дисгидротической экземы — местных, системных и физиотерапевтических.
В 2002 г. Swartling et al. впервые описали случай улучшения состояния пациентов с экземой рук, получивших инъекции ботулинического нейропротеина типа А Они опубликовали результаты исследования десяти пациентов с двусторонней дисгидротической экземой кистей на фоне повышенной потливости. На одной из кистей было проведено лечение onabotulinumtoxin A в дозировке 100 ЕД, восстановленных в 1,0 мл физиологического раствора, вторая выступала как контрольный образец. У семи из десяти пациентов отмечался хороший или очень хороший эффект от лечения. Klein et al. отреагировали на эту статью письмом, где отмечали, что терапевтический эффект от инъекций ботулинического нейропротеина типа А в отношении экземы рук, вероятно, не ограничивается уменьшением проявлений гипергидроза. Они предложили альтернативные объяснения терапевтическим результатам этого метода. Ботулинический нейропротеин может замедлять высвобождение нейротрансмиттеров и нейропептидов помимо ацетилхолина, в том числе вещества Р и кальцитонин-ген-связанного пептида. Также нейропротеин может непосредственно влиять на афферентные волокна, что потенциально может ингибировать сенсорную систему. Эти механизмы могут обосновать необходимость использования ботулинического нейропротеина типа А при экземе ладоней, не связанной с гипергидрозом, например в случае атопического дерматита.
Wollina и Karamfilov провели перспективное сравнительное контролируемое пилотное исследование с использованием местных кортикостероидов в сочетании с внутрикожными инъекциями 100 ЕД onabotulinumtoxin A, восстановленного в 2,0 мл физиологического раствора. К исследованию привлекли шесть пациентов. На обе руки были нанесены местные кортикостероиды, а на той стороне, где симптоматика была выражена сильнее, были добавлены инъекции ботулинического нейропротеина типа А Авторы наблюдали быстрое уменьшение зуда и дерматологических элементов с той стороны, где применялась комбинированная терапия. Они предположили, что лечебное действие ботулинического нейропротеина типа А при экземе объясняется не только ангидротическим эффектом, но и ингибированием вещества Р.
Ismail et al. Сосредоточились на хронической сухой экземе ладоней. Они провели перспективное нерандомизированное сравнительное исследование 30 случаев хронической двусторонней сухой экземы ладоней без признаков гипергидроза. Было выполнено сравнение по эффективности и переносимости комбинированной терапии эмолентами и местными кортикостероидами слабого действия на одной руке с тем же лечением, дополненным инъекцией 100 ЕД БНП интрадермально на другой руке, — с последующей оценкой как пациентами, так и специалистами в течение шести месяцев. Оба вида лечения оказались эффективны и хорошо переносились испытуемыми,однако улучшение, а также степень удовлетворённости пациентов оказались гораздо выше в случае, когда к обычной терапии были добавлены инъекции ботулинического нейропротеина типа А Кроме того, на стороне комплексного лечения значительно дольше сохранялся эффект (четыре месяца по сравнению с одним месяцем).
На сегодняшний день в литературе отсутствуют данные об исследованиях, посвящённых терапевтическому использованию ботулинического нейропротеина типа А при экземе подошв. Вероятно, причины этого те же, что и в случае с гипергидрозом подошв (болезненность, риск слабости стопы, необходимость использования большего количества ЕДиниц и, соответственно, более высокие расходы, а также меньшая эффективность по сравнению с областью ладоней и подмышек). Кроме того, концентрация препарата была бы иная, чем при гипергидрозе, а стандартные схемы пока отсутствуют.
ПОВЫШЕННАЯ ЖИРНОСТЬ КОЖИ
Shah провёл ретроспективный анализ среди 20 пациентов с целью изучить безопасность и субъективную эффективность интрадермальных инъекций ботулинического нейропротеина типа А в Т-зоне лица для уменьшения размера пор и выработки кожного сала. Основным ограничением исследования стало отсутствие объективного способа измерения выработки кожного сала. Оценка эффективности была основана исключительно на субъективной удовлетворённости пациентов и уменьшении размера пор кожи. Однако интересные находки этого предварительного исследования вдохновили Rose and Goldberg на новое перспективное исследование. Целью их работы стала оценка эффективности и безопасности интрадермальных инъекций ботулинического нейропротеина типа А для коррекции жирности кожи в области лба. В исследовании приняли участие 25 человек. Результат предлагалось субъективно оценить пациенту по шкале удовлетворённости и объективно — специалисту путём себометрических измерений. Также выполнялась фотосъёмка до и после процедуры. Каждый флакон abobotulinumtoxin A 300 ЕД восстанавливали в 3 мл физраствора и вводили препарат интрадермально в 10 точек лба по 3 – 5 ЕД, суммарно 30 – 45 ЕД. Авторы сообщают о значительном уменьшении выработки кожного сала и удовлетворённости 91 % пациентов.
Механизм, за счёт которого интрадермальные инъекции ботулинического нейропротеина уменьшают выработку кожного сала, пока не понят до конца, так как влияние ацетилхолина на сальные железы досконально не изучено. Вероятно, нейромодуляторный эффект БНП направлен прежде всего на гладкие мышцы, поднимающие волоски, и локальные мускариновые рецепторы. Li et al. показали, что сальные железы человеческой кожи in vivo и себоциты in vitro имеют на своей поверхности никотиновый ацетилхолиновый рецептор α7 (nAchRα7), соответственно ацетилхолин повышает синтез липидов дозозависимым образом. Исследователи привлекли 20 здоровых добровольцев к участию в двойном слепом плацебо-контролируемом исследовании на разных участках лица. Для оценки количества холинергических рецепторов в сальных железах проводился иммуногистохимический и иммуноцитофлуоресцентный анализ. После обработки одной стороны лица ботулиническим нейропротеином у добровольцев с жирной кожей наблюдалось с соответствующей стороны значительное уменьшение выработки кожного сала.
Принципиальное значение для эффективной терапии жирной кожи имеют техника выполнения инъекций и место введения препаратов. Чтобы гарантировать попадание в дерму, иглу вводят под углом 15° относительно кожи и оценивают появление капли препарата из близлежащих пор.
Shah et al. методом фотодокументирования обнаружили уменьшение размера пор, однако этот метод нельзя считать достоверным при оценке салообразования. Тем не менее, более ранние исследования показывают, что количество кожного сала в точности коррелирует с размером пор. Чтобы определить оптимальную технику выполнения инъекций, дозы и способы применения препарата для уменьшения жирности кожи и размера пор, потребуются дополнительные исследования.
В 2017 и 2019 годах были опубликованы два ретроспективных обзора, составленные Endly et al. и Shuo et al. Они заметили, что согласно большинству исследований интрадермальные инъекции ботулинического нейропротеина типа А уменьшают выработку кожного сала и размеры пор. Кроме того, пациенты чаще всего остаются довольны лечением, а существенных побочных эффектов не отмечается. Интрадермальная инъекция БНП может стать перспективным инновационным методом коррекции жирности кожи и других дерматологических проблем этого профиля, таких как увеличенные поры, акне и себорейный дерматит. Чтобы определить конкретные механизмы действия ботулинического нейропротеина типа А и подобрать оптимальные техники инъекций и дозировки при жирной коже и других подобных косметических проблемах, потребуются дополнительные исследования.
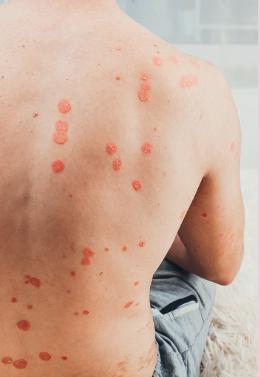
РИС. 4. Клиническая картина псориаза.
ПСОРИАЗ
Хотя для лечения псориаза (рис. 4) существует немало разных методов, в том числе терапия биологическими и синтетическими препаратами, научные изыскания продвинулись и в других направлениях. Был предпринят ряд исследований, призванных определить взаимоотношения между псориатическим расстройством и нервной системой, продемонстрировав высокую концентрацию нервных волокон в повреждённой псориазом коже, а также повышенный уровень кальцитонин-ген-связанного пептида и структурных белков, происходящих от сенсорных нервов. Эту гипотезу подкрепляет тот факт, что после утраты иннервации или нервной функции, либо повреждения нервной системы достигается ремиссия заболевания. Zanchi et al., а позже Aschenbeck, демонстрируя клиническое улучшение при инверсном псориазе после инъекций ботулинического нейропротеина типа А, предполагают, что он ингибирует нервную реакцию, инициируемую кальцитонин-ген-связанным пептидом и структурными белками. Гистологически процесс излечения псориаза показан Ward et al., которые на примере взрослой мыши KC-Tie2 (мышиная модель псориазиформного дерматита) отметили, что интрадермальные инъекции ботулинического нейропротеина типа А существенно снижают выраженность акантоза по сравнению с плацебо, а также уменьшают лимфоцитарную инфильтрацию. Однако клинических отчётов и обзорных статей на эту тему на данный момент опубликовано недостаточно, и они не являются плацебо-контролируемыми.
Zanchi et al. наблюдали клинические улучшения у 15 пациентов с инверсным псориазом, получивших инъекцию ботулинического нейропротеина типа А, но это исследование имело свои ограничения: результаты оценивались только самими пациентами (шкала VAS по зуду и болезненности), а также на основании сравнения фотографий. Поэтому Chroni et al. Раскритиковали данную работу по двум параметрам, а именно в связи с отсутствием количественной оценки улучшений (к примеру, по шкале PASI), а также гистологического анализа до и после лечения.
В материалах Saber и Gilbert представлены схожие результаты, но претензии к этим работам те же. В этих случаях авторы предположили, что положительное влияние ботулинического нейропротеина типа А связано с уменьшением локального потоотделения в складках кожи, например, как при болезни Хейли — Хейли (хронический доброкачественный семейный пемфигус). Однако пациенты также сообщали об уменьшении боли и зуда, вероятно потому, что БНП способен блокировать высвобождение алгогенных нейропептидов.
ВЫВОДЫ
Этот обзор подчеркивает большой потенциал применения инъекций ботулинического нейропротеина типа А при разных дерматологических заболеваниях. В настоящее время ещё не все молекулярные и патофизиологические ме- ханизмы, лежащие в основе его терапевтических эффектов, установлены. Можно сделать вывод, что состояние при многих заболеваниях, поражающих складки (инверсный псориаз, болезнь Хейли — Хейли, гидраденит), может быть улучшено путём инъекции ботулинического нейропротеина, вероятно, благодаря его ангидротическому эффекту, из‑за чего уменьшается мацерация кожи и риски присоединения вторичной инфекции.
Дальнейшие исследования должны быть направлены на изучение роли ботулинического нейропротеина типа А в регуляции нейропептидов и связи с нейроиммунной системой, чтобы лучше понять его терапевтический потенциал при ряде кожных заболеваний. Наконец, желательно разработать стандарты в отношении дозировки, степени восстановления и схемы инъекций для каждой нозологии.
Эффективность нейропротеина типа А при коррекции десневой улыбки
Афнан Аль-Фузан (Afnan F Al-Fouzan), отделение стоматологического протезирования, Стоматологическая школа при Университете Короля Сауда, Эр-Рияд, Саудовская Аравия
Ламия Моким (Lamia S Mokeem), Стоматологическая школа при Университете Короля Сауда, ЭрРияд, Саудовская Аравия
Рим Аль-Сакат (Reem T Al-Saqat), Стоматологическая школа при Университете Короля Сауда, ЭрРияд, Саудовская Аравия
Майса Альфалах (Maisa A Alfalah), отделение дерматологии, Медицинский комплекс им. Короля Абдулазиза, Эр-Рияд, Саудовская Аравия
Мана Альхарби (Mana A Alharbi), отделение дерматологии, Медицинская школа Исламского университета имама Мохаммада ибн Сауда, Эр-Рияд, Саудовская Аравия
Абдулла Аль-Самари (Abdullah E Al-Samary), отделение дерматологии, частная стоматологическая практика, ЭрРияд, Саудовская Аравия
ИСТОЧНИК Al-Fouzan AF, Mokeem LS, Al- Saqat RT, Alfalah MA, Alharbi MA, Al-Samary AE. Botulinum Toxin for the Treatment of Gummy Smile // J Contemp Dent Pract 2017;18(6):474-478.
Улыбка служит нам для выражения приятных эмоций. Её формируют три основных компонента: зубы, дёсны и губы. Немало исследований посвящено определению и измерению показателей, определяющих привлекательность улыбки. Большинство из них сводятся к тому, что идеальная высота десны, заметная при улыбке, должна составлять не более 3 мм. О десневой улыбке, то есть обнажении при улыбке излишнего количества верхней десны, можно говорить, когда имеется увеличенное расстояние между нижним краем верхней губы и верхним краем резцов. Это является одной из самых распространённых нежелательных косметических особенностей.
Со временем было разработано немало решений, призванных скорректировать этот дефект, — от сложных до самых простых. Для коррекции десневой улыбки в зависимости от индивидуальных особенностей применяют такие методы, как ортогнатические вмешательства (например, остеотомия по Ле Фор I и резекция кости), ортодонтическое лечение (интрузия резцов), удлинение коронок, гингивопластика, а также инъекции нейропротеина типа А.
Нейропротеин типа А используется для временного лечения десневой улыбки, когда последняя вызвана гиперфункцией мышц. Прежде всего следует определить вид десневой улыбки по области обнажения верхней десны (передняя, задняя, а также смешанный или асимметричный тип) либо по классификации Goldstein — низкая, средняя или высокая, в зависимости от степени обнажения десны. Эта классификация важна, так как позволяет определить степень задействования мышц и соответственно скорректировать технику инъекции нейропротеина типа А. Эффект проявляется через две недели и сохраняется 4 – 6 месяцев в зависимости от толщины и анатомии мышц.
Целью настоящего исследования была демонстрация успешного применения инъекций 100‑единичного нейропротеина типа А как консервативного метода коррекции десневой улыбки, вызванной гиперфункцией мимических мышц.
МАТЕРИАЛЫ И МЕТОДЫ
В исследовании приняли участие 23 пациентки с признаками десневой улыбки из‑за гиперфункции мышц. Из исследования были исключены пациентки с десневой улыбкой, вызванной малой высотой коронки зуба или длинной верхней челюстью, беременные или кормящие женщины, а также лица с нервно-мышечными расстройствами. В зоне воздействия применялась аппликационная анестезия под плёнку. Для инъекции 100‑единичного нейропротеина типа А, восстановленного в 1,0 мл 0,9 %-ного раствора хлорида натрия в соответствии с рекомендациями по разбавлению и хранению, использовался инсулиновый шприц с иглой калибра 30G. Препарат вводился на 3 мм латеральнее складки крыла носа, в месте прикрепления мышцы, поднимающей верхнюю губу и крыло носа. После инъекции пациенткам были даны указания: не ложиться, не заниматься физическими упражнениями, не массировать место инъекции в течение четырёх часов. Спустя две недели были сделаны фотографии в той же проекции.
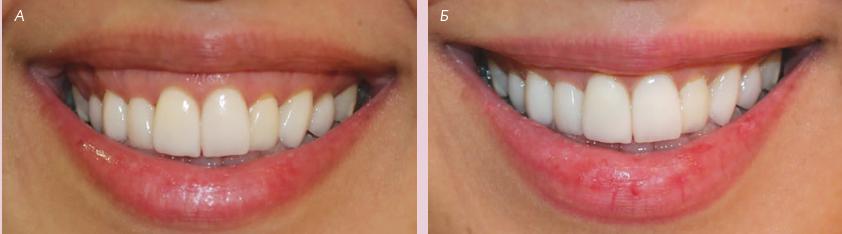
РИС. 1. Пациентка с десневой улыбкой, получившая инъекцию onabotulinumtoxin А, до (А) и после (Б) инъекции.
УЛУЧШЕНИЕ СОСТОЯНИЯ ДЕСНЕВОЙ УЛЫБКИ
Фотографии каждой пациентки загружались в компьютерную программу для расчёта изменения показателя обнажения десны (рис. 1). В каждом случае измеряли расстояние от нижнего края верхней губы до режущего края верхнего центрального резца во время улыбки до и после инъекции. Улучшение подсчитывалось по следующей формуле:

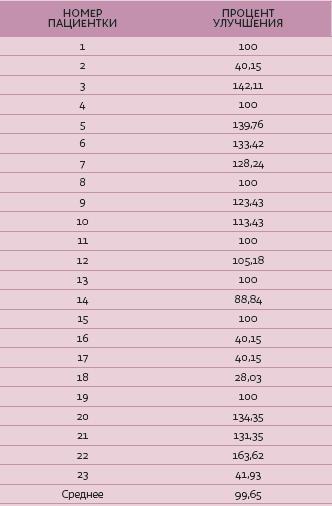
РЕЗУЛЬТАТЫ
Спустя две недели после инъекции onabotulinumtoxin А было отмечено существенное уменьшение высоты обнажающейся при улыбке десны по сравнению с исходным состоянием. Средний показатель улучшения (n = 23) составил 99,65 % (табл. 1). Сопутствующих нежелательных эффектов отмечено не было.
ОБСУЖДЕНИЕ
Улыбка — ключевой компонент невербальной коммуникации. Формируется она в два этапа — сначала верхняя губа приподнимается в сторону носогубных складок и слегка вжимается внутрь. Затем медиальные мышечные пучки приподнимают губу относительно передних зубов, а латеральные — относительно задних. Ограничением движения являются щёчные жировые компартменты латеральнее носогубной складки. На втором этапе за движение губы кверху отвечают три группы мышц: мышца, поднимающая верхнюю губу; большая скуловая мышца; верхние волокна щёчной мышцы.
Улыбка обнажает главным образом очертания губ, зубы и рельефную часть десны. Она может быть низкой, средней и высокой в зависимости от положения губ. Согласно Ezquerra et al., улыбка считается низкой, если под верхней губой видна лишь часть зубного ряда. Если видно 1 – 3 мм десны, улыбку называют средней, если больше 3 мм — высокой. Было показано, что самой привлекательной считается улыбка, при которой обнажается 0 – 2 мм десны. В другом исследовании, проведённом Peck et al., выявлено, что средний и высокий тип улыбки встречаются более чем у 75 % людей в популяции. В том же исследовании авторы подметили, что имеет значение также гендерный фактор. Низкая улыбка, как выяснилось, чаще встречается у мужчин, чем у женщин, в соотношении 2,5 : 1. Согласно Peck et al., такая улыбка выглядит наименее привлекательно. Высокая же линия улыбки чаще встречается у женщин — соотношение 2 : 1.
Silberberg et al. обнаружили, что излишнее обнажение десны наблюдается примерно у 10 % населения. Это соответствует выборке данного исследования. Пиковый возраст для проявления этой проблемы составляет 20 – 30 лет, а затем частота встречаемости постепенно уменьшается, поскольку мышцы верхней губы теряют свой тонус. Гингивальная или десневая улыбка может быть вызвана излишней высотой верхних дёсен; гиперфункцией мышцы, поднимающей губу; задержкой прорезывания зубов. Первое диагностируется посредством оценки костных компонентов улыбки. Второе имеет место, если скелетные параметры верхней челюсти в норме, но при улыбке видно 2 мм десны. Последний вариант диагноза применим, если бoльшая часть коронки зуба закрыта десной вследствие аномального развития зубов.
Для дифференциальной постановки диагноза требуется тщательный осмотр и сбор анамнеза. Выявление десневой улыбки должно производиться путём проверки симметрии и пропорций черт лица как во фронтальной, так и в боковой проекции. Для разных причин возникновения десневой улыбки разработаны разные методы лечения. К примеру, при скелетном дисбалансе подойдут ортогнатическая хирургия и ортодонтическое лечение. При позднем пассивном прорезывании уместно будет пародонтологическое лечение. Наконец, гиперфункцию мышц долгое время лечили посредством пластической реконструктивной хирургии. Инъекции нейропротеина типа А стали использовать сравнительно недавно. С распространением эстетической медицины многие пациенты получили надежду обрести идеальную улыбку минимально инвазивным способом. Silberberg et al., изучив, из чего складывается максимально привлекательная улыбка, пришли к выводу, что её определяют:
- минимум обнажения десны;
- симметричность и гармония линии верхней десны и верхней губы;
- здоровье десневой ткани в межзубных областях;
- гармоничность сочетания передних и задних сегментов зубов;
- правильная анатомия и пропорции зубов;
- здоровый цвет и оттенок зубов;
- ход нижней губы параллельно режущим краям передних верхних зубов.
При этом десневая улыбка — один из самых смущающих пациента эстетических недостатков. Применяемые ранее методы коррекции, такие как остеотомия по Ле Фор I, резекция кости, удлинение коронок, гингивэктомия, не были популярны среди пациентов, так как они часто дают осложнения, дороги и требуют длительного периода лечения. К примру, остеотомия по Ле Фору I в трудных случаях может нарушить проходимость носовых ходов. Появление нейропротеина типа А в косметической стоматологии оказалось весьма ценным приобретением.
Сравнительно недавно ботулинотерапия была отнесена к основным методам коррекции десневой улыбки, поскольку она удобна и безопасна, риски невысоки и обратимы. Важнее всего, пожалуй, быстрота проявления эффекта. Сохраняется же он от четырёх до шести месяцев, в зависимости от активности и толщины мышц. Степень уменьшения проявлений десневой улыбки может существенно варьироваться, что согласуется с результатами исследования Durgekar et al. Как упоминают в своей статье Pecket al., у пациентов с десневой улыбкой наблюдается на 20 % более высокая активность мышц периоральной области, из‑за чего эффект нейропротеина типа А проходит быстрее.
В рамках данного исследования побочных эффектов не наблюдалось. В некоторых случаях при неправильной технике инъекции возникает неестественное асимметричное растяжение губ. Эффект от введения нейропротеина типа А может помешать правильно произносить некоторые звуки, иногда вызывает асимметрию верхней губы, а также осложняет процесс поцелуя, как сообщают Sandler et al.
ЗАКЛЮЧЕНИЕ
Инъекции нейропротеина типа А являются эффективным временным консервативным методом коррекции десневой улыбки. Они позволяют уменьшить её проявления и улучшить состояние мышц, участвующих в формировании улыбки. Ботулинотерапия позволяет безопасно корректировать степень обнажения десны при условии подбора подходящей дозы и условий инъекции.
Экспертное мнение

О. Р. Орлова, д. м. н., профессор, президент Межрегиональной общественной организации специалистов ботулинотерапии (МООСБТ), директор Центрального института ботулинотерапии и актуальной неврологии (ЦИБиАН), г. Москва
Дорогие коллеги!
Представленный номер дайджеста открывается уникальной публикацией — систематическим обзором литературы по применению ботулинического нейропротеина в лечении дерматологических синдромов. Так уж исторически сложилось, что косметологи, имея базовое дерматологическое образование, используют ботулинотерапию в основном с эстетической целью, а дерматологи пока незаслуженно мало пользуются всеми уникальными возможностями ботулинотерапии.
Эссенциальный гипергидроз справедливо отнесён авторами статьи к кругу возможно наследственных вегетативных синдромов, а ботулинотерапия — к методам лечения первой линии. Дозы БТА, размер иглы, объём растворителя, анестезия могут быть различными, но эффект в большинстве случаев выраженный и продолжительный. Поскольку у одного пациента могут быть вовлечены разные зоны тела (подмышки, ладони, стопы, голова и лицо), то общая доза БТА может быть значительной, что иногда приводит к временным системным побочным эффектам. Отмечено, что лечение гипергидроза стоп наименее эффективно.
Хромгидроз и бромгидроз - редкие синдромы, но ботулинотерапия эффективна, несмотря на то что в этих случаях мишень БТА — не ацетилхолин, а другие медиаторы. Это еще раз доказывает, что БТА является универсальным пресинаптическим блокатором всех видов трансмиссии, и его терапевтический потенциал уникален.
Дисгидротическая экзема и псориаз патогенетически наименее понятные заболевания, но эффективность ботулинотерапии позволяет предположить нейрогенные механизмы кожных проявлений.
Наконец, применение БТА в лечении эритемы, приливов и жирности кожи должно войти в повседневную практику косметологов и дерматологов.
Еще одна публикация посвящена лечению десневой улыбки. Этот аспект междисциплинарной стоматологии уже освещался на страницах Дайджеста, но данная публикация интересна тем, что авторы приводят способы объективизации полученного результата, а также с уверенностью отмечают, что ботулинотерапия является методом первого выбора, в противовес устаревшим травматичным хирургическим методам коррекции десневой улыбки.



 Сайт может содержать материалы, предназначенные для лиц старше 18 лет
Сайт может содержать материалы, предназначенные для лиц старше 18 лет
